- Life
- Forschung
Meldung vom: | Verfasser/in: Friederike Gawlik
Das Toxin Candidalysin des Hefepilzes Candida albicans ist während einer Infektion in eine ungewöhnliche Proteinstruktur eingebunden, deren Aufbau die Wissenschaft bislang vor ein Rätsel stellte. Nun gelang es Forschenden des Leibniz-Instituts für Naturstoff-Forschung und Infektionsbiologie (Leibniz-HKI), die Funktion der ungewöhnlichen Anordnung zu entschlüsseln. Durch Veränderungen an der Proteinstruktur konnte auch die Pathogenität des Pilzes vermindert werden. Die neuen Erkenntnisse wurden genutzt, um das Pilztoxin mit Hilfe von künstlichen Antikörpern unschädlich zu machen. Damit eröffnet sich ein neuer Weg, hartnäckige Formen der vaginalen Candida-Infektion zu therapieren.
Ein opportunistischer Pilz
Der Hefepilz Candida albicans ist Bestandteil des menschlichen Mikrobioms und lebt normalerweise im Gleichgewicht mit anderen Mikroorganismen. Wird diese Balance jedoch gestört, kann der Pilz unkontrolliert wachsen und Infektionen verursachen. Als „Scheidenpilz“ betrifft C. albicans jedes Jahr Millionen Frauen weltweit. In einigen Fällen versagt die antimykotische Behandlung und es kommt zu chronischen, wiederkehrenden Pilzinfektionen, die die Lebensqualität der Betroffenen erheblich einschränken und einen großen Leidensdruck verursachen.
In faltigem Gewand
Das von dem Pilz ausgeschiedene Toxin Candidalysin ist für Zellschädigungen im menschlichen Gewebe verantwortlich. Bei einer vaginalen Infektion sind typischerweise heftige Entzündungsreaktionen die Folge, die dem Pilz jedoch nur wenig ausmachen. Stattdessen erhöht sich die Schwere der Erkrankung.
Candidalysin ist vor der Freisetzung in ein Vorläuferprotein mit dem Namen Ece1 eingebettet: Insgesamt acht Peptidsequenzen bilden hierbei eine aufgefaltete Struktur, die für solche Toxine sehr unüblich ist. Unklar war bisher, warum das Toxin in diese außergewöhnliche Struktur integriert ist und welche Rolle die einzelnen Bestandteile dabei spielen. In einer soeben in Nature Microbiology veröffentlichten Studie untersuchte ein internationales Team aus Forschenden des Leibniz-HKI, des Institut Pasteur Paris, des King’s College in London, der University of Wisconsin sowie des Leibniz-Forschungszentrums Borstel deshalb die Struktur von Ece1 sowie bestimmte Peptide daraus, bekannt als NCEPs (Non-Candidalysin-Ece1-Peptides).
Bei fast allen mikrobiellen Peptidtoxinen müssen die produzierenden Zellen Vorsichtsmaßnahmen gegen eine Selbstvergiftung treffen. Freies Candidalysin bildet hier eine Ausnahme, es schädigt die eigenen Pilzzellen nicht. Demnach kann dessen Einbettung in das komplexe Vorläuferprotein Ece1 nicht mit einem Selbstschutz der Pilzzelle erklärt werden. Der Grund für die ungewöhnliche Struktur von Ece1 muss also ein anderer sein.
In weiterführenden Experimenten konnten die Forschenden zeigen, dass das Toxin extrem zur Selbstaggregation und Verklumpung neigt. Daraufhin veränderten die Forschenden die Ece1-Struktur, wodurch die korrekte Faltung des Proteins gestört wurde. Diese Manipulation hemmte im Laborversuch die Bildung der Pilzhyphen von Candida albicans, was auch die Freisetzung von Candidalysin beeinträchtigte: das Toxin verklumpte in den Zellen und wurde unwirksam. „Unsere Ergebnisse deuten darauf hin, dass jedes einzelne Peptid im Ece1-Vorläuferprotein für die Freisetzung von Candidalysin notwendig ist. Die Hauptfunktion des Vorläuferproteins ist offenbar, eine Verklumpung des Toxins zu verhindern“, erklärt Erstautorin Rita Müller. „So können die Pilzzellen, die Hyphen, normal funktionieren, während das Toxin problemlos zu den Wirtszellen gelangen und dort Schaden anrichten kann“, ergänzt die zweite Erstautorin Annika König.
Mit Nanokörpern gegen das Toxin
In einer weiteren, im Journal mBio veröffentlichten Studie konzentrierten sich die Forschenden auf eine neue Strategie zur Neutralisation von Candidalysin: die Anwendung von Nanokörpern.
Nanokörper sind synthetisch hergestellte Antikörper. Ursprünglich wurden sie aus dem Blut von Kamelen oder Lamas gewonnen. Sie sind viel kleiner und einfacher strukturiert als ihre menschlichen Pendants, dies macht sie wesentlich flexibler als humane Antikörper. So sind Nanokörper in der Lage, sich ganz spezifisch an diejenigen Bindungsstellen der Erreger anzudocken, mit denen sich diese an die Wirtszellen anheften. Auf diese Weise blockieren sie den Weg für die Erreger und verhindern eine Infektion. Dieses Prinzip wurde nun erstmals genutzt, um Candidalysin unschädlich zu machen.
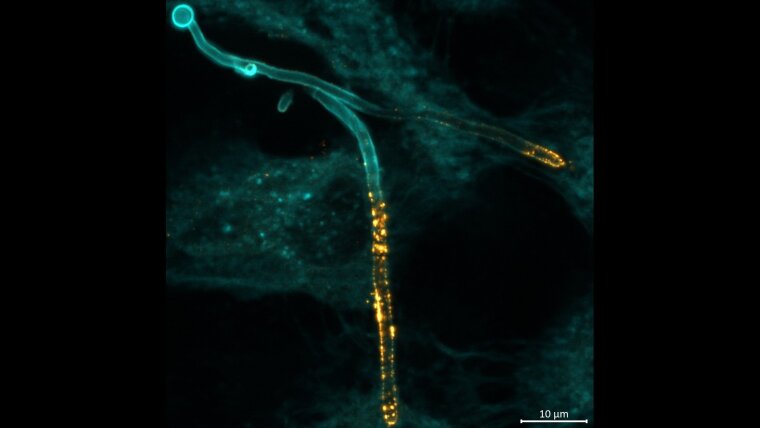
Bei vaginalen Infektionen mit Candida albicans verursacht Candidalysin Schäden im Schleimhautgewebe und fördert so entzündliche Überreaktionen des Immunsystems, die zur Verschlechterung der Symptome beitragen. Insbesondere für die chronische, wiederkehrende Form der vaginalen Candidose sind die Behandlungsmöglichkeiten derzeit nur sehr begrenzt. Dabei trifft diese Erkrankung weltweit jährlich etwa 138 Millionen Frauen. Die Forschenden untersuchten deshalb die Wirkung von Nanokörpern auf die Pilzinfektion. In Laborversuchen konnte gezeigt werden, dass spezielle Nanokörper die Aktivität von Candidalysin tatsächlich blockieren können. Dabei reduzierten die Nanokörper im Labor Toxin-bedingte Gewebeschäden sehr effektiv, was auch entzündliche Folgereaktionen hemmen würde. Die Nanokörper wurden von den Forschenden mittels eines speziellen Mikroskopie-Verfahrens – der Immunfluoreszenz – direkt an den von den Pilzhyphen besiedelten Gewebestellen lokalisiert. Mit Hilfe von weiteren Modellierungen im Labor und am Computer war es außerdem möglich, Vorhersagen zur Dosierung und zum Zeitpunkt der Nanokörperzugabe zu treffen, um das Toxin zu neutralisieren.
Nanokörper, die gegen Candidalysin gerichtet sind, könnten also bei der Behandlung von komplizierten wiederkehrenden Fällen der vaginalen Candidose hilfreich sein. Bei einem Vergleich mit dem häufig verwendeten Antimykotikum Fluconazol zeigte sich, dass die Kombination beider Therapieformen besonders effektiv ist. „Zusammen mit diesem Antipilzmedikament könnte der Einsatz von Nanokörpern also eine echte Behandlungsoption für die Erkrankung darstellen“, betont Erstautorin Marisa Valentine. „Indem man Candidalysin neutralisiert, werden die hyperinflammatorischen Symptome gelindert. Dies könnte für viele Patientinnen von großer Bedeutung sein“, so ihr Kollege Paul Rudolph, ebenso Erstautor der Studie.
Die genannten Wissenschaftlerinnen und Wissenschaftler arbeiten unter der Leitung von Bernhard Hube und Marc Thilo Figge im Rahmen ihrer Dissertation am Candidalysin und dessen Einfluss auf das Infektionsgeschehen. Hube ist Abteilungsleiter für Mikrobielle Pathogenitätsmechanismen, Figge ist Gruppenleiter für Angewandte Systembiologie am Leibniz-HKI. Beide sind Professoren an der Friedrich-Schiller-Universität Jena. Die Arbeiten wurden unter anderem im Rahmen des Exzellenzclusters Balance of the Microverse vom Freistaat Thüringen, der Deutschen Forschungsgemeinschaft (DFG), dem Bundesministerium für Bildung und Forschung (BMBF) und der Europäischen Union gefördert und darüber hinaus durch den Wellcome Trust, die National Institutes of Health (NIH) sowie das Horizon 2020 Netzwerk FunHoMic der EU unterstützt.
Original-Publikationen:
Müller R, König A, Groth S, Zarnowski R, Visser C, Handrianz T, Maufrais C, Krüger T, Himmel M, Lee S, Priest EL, Yildirim D, Richardson JP, Blango MG, Bougnoux ME, Kniemeyer O, d’Enfert C, Brakhage AA, Andes DR, Trümper V, Nehls C, Kasper L, Mogavero S, Gutsmann T, Naglik JR, Allert S, Hube B (2024) Secretion of the fungal toxin candidalysin is dependent on conserved precursor peptide sequences. Nature Microbiology, https://doi.org/10.1038/s41564-024-01606-zExterner Link
Valentine M, Rudolph P, Dietschmann A, Tsavou A, Mogavero S, Lee S, Priest EL, Zhurgenbayeva G, Jablonowski N, Timme S, Eggeling C, Allert S, Dolk E, Naglik JR, Figge MT, Gresnigt MS, Hube B (2024) Nanobody-mediated neutralization of candidalysin prevents epithelial damage and inflammatory responses that drive vulvovaginal candidiasis pathogenesis. mBio, https://doi.org/10.1128/mbio.03409-23Externer Link
Beutenbergstraße 11a
07745 Jena Google Maps – LageplanExterner Link
Beutenbergstraße 11a
07745 Jena Google Maps – LageplanExterner Link